7 101,00 ₽
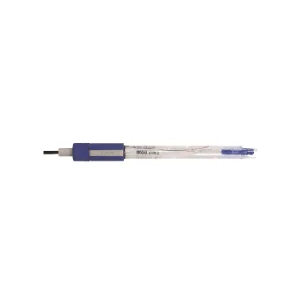
Электрод стеклянный лабораторный для измерения pH ЭСЛ-15-11. Диапазон измерения до 14 рН, температура анализируемой среды от +25 до +100°С. Запаянная конструкция с высокой стабильностью параметров. Без кабеля со специальным разъемом для подключения.
Цена зависит от курса валют. Пожалуйста, уточняйте цену, связавшись с нами любым удобным Вам способом.
Электрод стеклянный лабораторный для измерения pH ЭСЛ-15-11 — малогабаритный электрод без кабеля со специальным разъемом для подключения. Предназначен для измерения величины pH в лабораторных условиях. Электроды имеет запаянную конструкцию с высокой стабильностью параметров. Электростатический экран защищает электроды от внешних электрических полей.
Стеклянные электроды — тип ионоселективных электродов, сделанных из легированных стеклянных мембран, которые чувствительны к специфическим ионам, используемые для определения концентрации ионов в растворе. Важная часть приборов химического анализа и физико-химических исследований.
В современной практике широко применяются мембранные ионоселективные электроды (ИСЭ, в том числе и стеклянные), являющиеся частью гальванического элемента. Электрический потенциал электродной системы в растворе чувствителен к изменению содержания определённого вида ионов. Это выражается и в зависимости электродвижущей силы (ЭДС) гальванического элемента от концентрации этих ионов.
Стеклянный электрод ЭСЛ-15-11 создает второй потенциал на мембране, разделяющей стандартный HC и тестируемые растворы . Мельчайший ток, необходимый для рН-метра, создает в растворах двойной слой. Он вызывает ионный обмен на внутренней и внешней поверхностях и вызывает диффузию ионов через стеклянную мембрану.
| Параметр | ЭСЛ-15-11 |
| Диапазон измерения рН при 25 ºС | 0 … 14 рН |
| Температура анализируемой среды | 25 … 100 °С |
| Координаты изопотенциальной точки | рНи = 4,25 рН, Еи = -25 мВ |
| Электрическое сопротивление при 20 °С, Мом | (500 ± 250) |
| Индикаторная часть электрода | Специальное стекло |
| Габаритные размеры электрода, не более | |
| — диаметр погружной части электрода | 8,25 мм |
| — длина электрода | 130 мм |
| — кабель, длина | нет |
| Разъем | Специальный |
Стеклянные электроды — наиболее распространенные электроды. С помощью данного вида электродов определяют рН растворов. Существуют стеклянные электроды, которые позволяют определить концентрацию ионов Na+, K+. В основе теории стеклянного электрода лежит представление о том, что стекло — это ионообменник, который может вступать в ионообменное взаимодействие с раствором. Стекло при этом рассматривается как твердый электролит.
Стекло, состоящее из окислов натрия, кальция, кремния, обладает резко выраженным специфическим сродством к ионам Н+. Вследствие этого при соприкосновении с водными растворами в поверхностном слое стекол образуется слой, в котором ионы Na+ оказываются почти полностью замещенными на ионы Н+. Поэтому мембранный электрод, изготовленный из такого стекла, обладает Н+-функцией.
Введение в состав стекла окислов бария, цезия, лантана и замена натрия на литий значительно расширяет диапазон Н+-функции стеклянного электрода. Введение же окислов алюминия и бора значительно снижают Н+-функции стеклянного электрода. Таким путем удалось создать ионселективные стеклянные электроды для ионов Na+, K+, Li+, Ag+. Продолжительность функционирования стеклянного электрода определяется рядом факторов — состав стекла, толщина рН-чувствтельного поверхностного слоя мембраны. Сюда же относятся температура и состав раствора, в котором электрод используется.
Разрушение стекла водными растворами происходит в результате сорбции воды стеклом и глубокое ее проникновение в толщу. Коррозионному действию щелочных растворов, образующихся при экстракции щелочных компонентов стекла, подвергается и горловое стекло. Кремнекислородная сетка испытывает воздействие с обеих сторон мембраны. В конце концов развиваются трещины, приводящие к нарушению функции электрода. Для защиты электрода от разрушения необходимо хранить его в воде, так как в воде происходит выщелачивание связанных ионными силами основных компонентов стекла и замена их ионами водорода. В результате этого на поверхности стекла образуется слой гидролизованного кремнезема, предохраняющий стекло от дальнейшего разрушения.





Пожалуйста, заполните форму. Ответим в течение 30 минут
Компания КОЛБА поздравляет всех женщин с 8 Марта!
Пусть внимание и подарки радуют вас каждый день, а 8 марта будет днём генеральной репетиции!
Спасибо за длинные выходные.
По всем заявкам ответим 10 марта.
Мы используем необходимые файлы cookie, для работы нашего сайта.
Продолжая использовать сайт, вы соглашаетесь с использованием файлов cookie на нашем сайте в соответствии с нашей политикой конфиденциальности.