27 779,00 ₽
HI3843 — это набор для химических тестов на основе титрования, который определяет концентрацию гипохлорита в диапазоне от 50 до 150 г/л.
Цена зависит от курса валют. Пожалуйста, уточняйте цену, связавшись с нами любым удобным Вам способом.
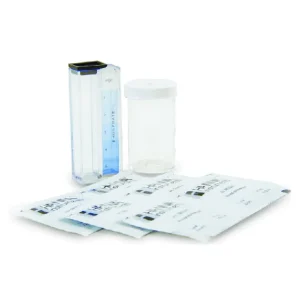
HI3843 — это набор для химического анализа, который измеряет содержание гипохлорита методом йодометрического титрования. Прибор HI3843 поставляется в комплекте со всеми реагентами и оборудованием, необходимыми для проведения примерно 100 тестов.
| Тип | титрирование |
| Наименьшее приращение | 5 г/л (ppt) |
| Метод | йодометрический |
| Количество тестов | 100 в среднем |
| Информация для заказа | Тестовый набор HI3843 включает 30 мл раствора йодида калия, 100 упаковок отбеливающего реагента B, 60 мл отбеливающего реагента C (2), 125 мл стеклянной колбы Эрленмейера и 1 мл пластиковых пипеток (25) |
| Реагент | HI3843-100 |
| Диапазон содержания гипохлорита | 50-150 г/л (ppt) |
Важность применения набора для тестирования на гипохлориты:
Гипохлориты являются распространенными отбеливающими агентами. Они используются для отбеливания текстиля и бумаги, а также для дезинфекции растворов. Раствор гипохлорита натрия традиционно используется для обработки воды в бассейне, поскольку это недорогая и легкодоступная форма хлора. Раствор обычно содержит от 10 до 15% доступного хлора (что эквивалентно 100-150 г/л), но он быстро теряет свою силу при хранении. Кроме того, поскольку он сильно подвержен влиянию тепла, света, pH и тяжелых металлов, его необходимо регулярно контролировать.
В тестовом наборе HI 3843 используется метод йодометрического титрования. Раствор гипохлорита обрабатывают йодидом калия и сильно подкисляют кислотой (Этап 1). Количество образующегося йода эквивалентно хлору в образце. Затем концентрацию йода рассчитывают титрованием тиосульфат-ионов, которые восстанавливают йод обратно до ионов йодида (шаг 2).
Шаг 1: OCl + 2H + 2I → Cl + I—+——2 + Ч2O
Шаг 2: Я2 + 2(С2O3)2- → 2I + (S—4O6)2-

Пожалуйста, заполните форму. Ответим в течение 30 минут
Компания КОЛБА поздравляет всех женщин с 8 Марта!
Пусть внимание и подарки радуют вас каждый день, а 8 марта будет днём генеральной репетиции!
Спасибо за длинные выходные.
По всем заявкам ответим 10 марта.
Мы используем необходимые файлы cookie, для работы нашего сайта.
Продолжая использовать сайт, вы соглашаетесь с использованием файлов cookie на нашем сайте в соответствии с нашей политикой конфиденциальности.